バクテリオファージは抗生物質の素晴らしい代替薬なのですが、現時点では大勢の患者に提供することができません。バクテリオファージ治療を行う医療施設が世界中に設立され、治療に使えるバクテリオファージのデータが完成しなければ、現実の医療で広く使うことは難しいでしょう。現時点でバクテリオファージ治療を受けることは難しく、実現の可否は各国の規制当局や政治家、巨大製薬企業が変化を望むかどうかにかかっています。
抗生物質の代替薬となる可能性があるもの
薬剤耐性菌が脅威となっている現状を打開する技術が求められています。抗生物質の代替薬がなければ、傷からの感染や昆虫の咬傷が死を意味する時代が再びやってくるかもしれません。
抗生物質の代替薬はまだ十分には開発されていません。新しく改良された抗生物質だけが束の間の効果を発揮しています。しかし、ほとんど場合、すぐに薬剤耐性菌が現れてしまいます。ときには新しい抗生物質が販売される前に薬剤耐性菌が現れることもあります。
人類にとって本当に必要なのは、病気の原因となる細菌だけを標的として作用し、マイクロバイオームを傷つけることのない成分を持つ抗生物質です。細菌が薬剤耐性を獲得しにくい成分であれば理想的です。
- ペプチド
- バクテリオファージ
- エンドリシン
- 新規エンドリシン
ペプチド

ダプトマイシンとコリスチンはよく知られている抗生物質ぺプチドです。ダプトマイシンは2003年に導入された最新のぺプチドで、ブドウ球菌や腸球菌などのグラム陽性細菌に対して効果があります。
コリスチンは1959年に使われ始めましたが、腎毒性が強いため現在ではほとんど使われていません。アシネトバクターや緑膿菌、クレブシエラなどの高薬剤耐性を持つグラム陰性細菌に対する最後の手段として使われています。
これら二つの抗生物質ぺプチドはそこまで頻繁に使われているわけではありませんが、すでに薬剤耐性が発生しています。あるアメリカ人女性が亡くなった原因は、感染した細菌が最終手段であるコリスチンも含めた26種類の抗生物質に耐性を持っていたからでした。
他の抗生物質ペプチド(AMP)は、植物や哺乳動物において細菌やウイルスと戦うための防御機構として自然に産生されます。その薬効範囲は非常に幅広く、細菌やウイルスに対応してさまざまに変化します。
AMPの作用機序はまだ詳しくは分かっていません。AMPは細菌の細胞膜を崩壊させ、浸透圧を高めることで細胞の逸出や溶解を引き起こします。また、AMPは細胞内の標的と相互作用することで、細胞代謝に干渉している可能性もあります。
AMPを使用する際の大きな懸念は、薬効範囲が広いにも関わらず薬剤耐性が発達することです。特に、AMPが自然免疫系に由来している場合は、定期投与のリスクが大きくなります。自然免疫系由来のペプチドを頻繁に投与して薬剤耐性菌が発生すると、この耐性菌は人間の免疫系に対して耐性を持っていることになるため、非常に危険です。感染症が抗生物質で治療された後、次に何が起こるのかはもうお分かりだと思います。
非常に強力な薬剤耐性菌の誕生です!
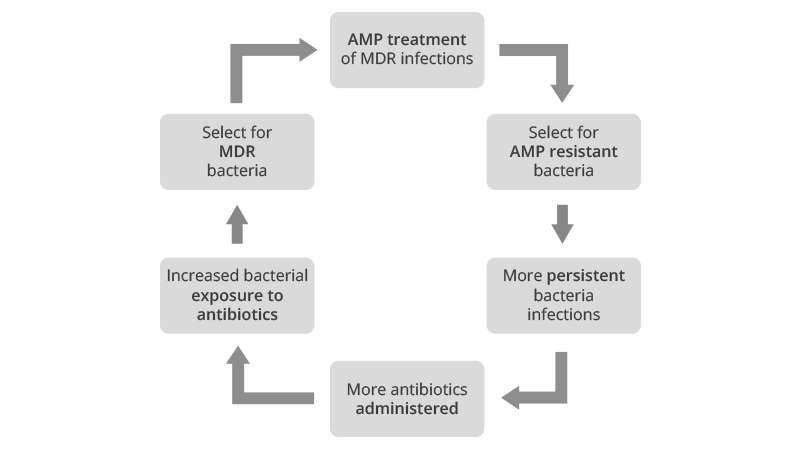
ペプチドが抗生物質の抱える問題の解決策でないことは明らかです。
では他に何が残されているのでしょうか?
バクテリオファージ
「敵の敵は味方」
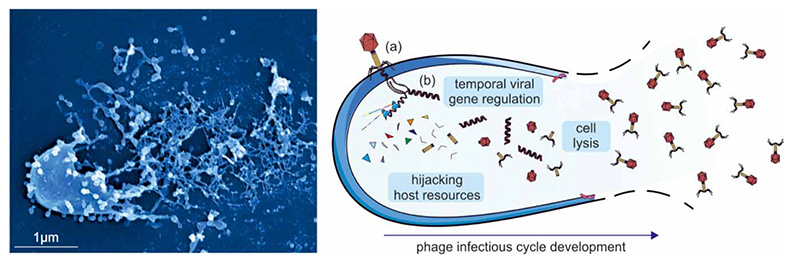
バクテリオファージは細菌だけを攻撃するウイルスです。外部環境中や植物や哺乳動物の体内など、細菌がいる場所であればどこにでも存在しています。数十億年の間、バクテリオファージは細菌とともに進化してきました。バクテリオファージは細菌に対して非常に選択的に作用します。溶菌性ファージは細菌のDNAに感染し、細菌が新しいバクテリオファージを生み出すように再プログラムします。十分な数のバクテリオファージが生み出されると、今度はバクテリオファージのDNAからエンドリシンと呼ばれる「ハサミ」がつくられ、細菌の細胞壁を切り崩してしまいます。細胞壁が崩れた細菌が破裂すると、バクテリオファージは再び自由に動き出します。そして次の標的となる細菌に向かい、すべての細菌が死滅するまで同じプロセスを繰り返します。標的となる細菌が存在しなくなると、バクテリオファージは体外に出ていくか、新しい細菌が現れるのを待ち構えます。
バクテリオファージは素晴らしい働きをします。実際、抗生物質の代替薬候補の一つと言えます。
1. バクテリオファージは非常に選択的です。「選択的」とは感染症を起こす細菌とだけ戦い、他の善玉共生菌は攻撃しないことを意味します。
2. バクテリオファージは標的となる細菌すべてが死滅するまで増殖を続けます。
3. バクテリオファージは人間の体の細胞を攻撃しないため、副作用が起こりません。
4. バクテリオファージは簡単に産生することができます。
ファージセラピーには100年以上の歴史があります
ファージセラピーはフランスで1917年にフェリックス・デレーユという人が始めました。今日でも東ヨーロッパの一部で行われています。ジョージアのトビリシでは、デレーユとジョージ・エリアヴァによってファージ治療の施設(設立者にちなんで「エリアヴァ」と呼ばれています)が設立されました。現在でも、エリアヴァでは患者がファージ治療を受けており、成功を収めています。
ではなぜバクテリオファージが話題となることがなく、関連製品が販売されていないのでしょうか?
それには理由がいくつかあります。
1. 現在では抗生物質が使われているため、代わりとなる治療法が必要とされていない。誰も抗生物質が人間の体に及ぼす危険性に気付いていない。
2. 製薬会社がバクテリオファージに関心を持っていない。バクテリオファージは自然発生するものなので特許を取得することができず、製薬会社は大きな利益を得ることができない。
3. バクテリオファージに対する耐性が非常に早く発生する。ただし、各々の細菌に対して10タイプのバクテリオファージが存在するため、耐性の発生は問題ではありません。問題は、感染を引き起こす細菌と戦うバクテリオファージを見つけなければいけないことなのです!
敗血症や急性呼吸器感染症のような重篤な感染症では、感染源の細菌株をすぐに特定する必要があり、時間がかかることは大きな問題となります。また、複数の細菌株によって引き起こされる感染症も、適切なマイクロファージの組み合わせを見つけるために時間がかかります。
4. バクテリオファージは感染源の細菌のDNAを「利用」しますが、これは望ましくない影響を与える可能性もあります。例えば、比較的害の少ない大腸菌を危険な腸管出血性大腸菌に変化させてしまう可能性があります。
バクテリオファージ治療は個々の患者に合わせたオーダーメイド治療です。新しい医薬品の承認には数年の時間と数億円の費用がかかります。ヨーロッパやアメリカの規制当局で適切な承認プロセスを受けていては、患者にとって意味のある治療を行うことは不可能です。
東ヨーロッパではバクテリオファージ治療の膨大な量の経験が蓄積されているのですが、蓄積されたデータは西側諸国の保健医療の基準を満たしていません。したがって、現時点ではこれらのデータはヨーロッパや米国の規制当局から承認を得るのには役立ちません。バクテリオファージ治療は、一般的に利用可能な他の薬剤(抗生物質)で効果が得られなかった場合にだけ、オーダーメイド治療として利用できます。それ以外には、ジョージアのトビリシまで行くしかありません。
エンドリシン
バクテリオファージからエンドリシンの話に移りましょう。 エンドリシンは、バクテリオファージが細菌の中で増殖したのち、細菌の細胞を溶解するために用いる道具です。20世紀初頭にエンドリシンの研究が盛んになりました。エンドリシンは細菌の細胞外皮を切り落とし、細菌を溶解させます。バクテリオファージは細菌を内部から分解しますが、バイオ技術によって生産されたエンドリシンは細菌の外部からも細菌を攻撃します。これは特に黄色ブドウ球菌や腸球菌などのグラム陽性細菌に効果的です。これらの細菌の持つ細胞壁は外部から容易に接触できるからです。対照的に、外部膜層を持つグラム陰性細菌の細胞壁はエンドリシンに対して強固です。
エンドリシンは効果的かつ選択的に素早く作用し、マイクロバイオームを傷つけることがありません。また、高度薬剤耐性菌や慢性感染症の休眠中の(常在)細菌にも効果があります。
エンドリシンの有効性はすでに複数の動物モデルや食品への応用で示されています。
地球上に存在するすべての細菌それぞれに対して10タイプのバクテリオファージが存在し、各々のバクテリオファージは特有のエンドリシンの遺伝子を有しています。このことは、地球上のすべての細菌に対して、それらを排除するためのエンドリシンが存在していることを暗示しています。
エンドリシンには以下の利点があります。
- エンドリシンは選択的で、感染を引き起こす細菌のみ死滅させる
- エンドリシンは高度薬剤耐性菌や常在菌にも効果がある
- 堅固な細胞壁にも効果があるため、細菌がエンドリシンに対して耐性を発達させるのが困難
すでに触れたとおり、エンドリシンの難点の一つはグラム陽性細菌にだけ効果があることです。頻繁に現れる薬剤耐性菌は、緑膿菌やアシネトバクター・バウマニ、クレブシエラ・ニューモニエなどのグラム陰性細菌なのです!
従って、エンドリシンは抗生物質の代替薬として優れているのですが、すべての問題を解決してくれるわけではありません。
私たちには新しいエンドリシンが必要です。
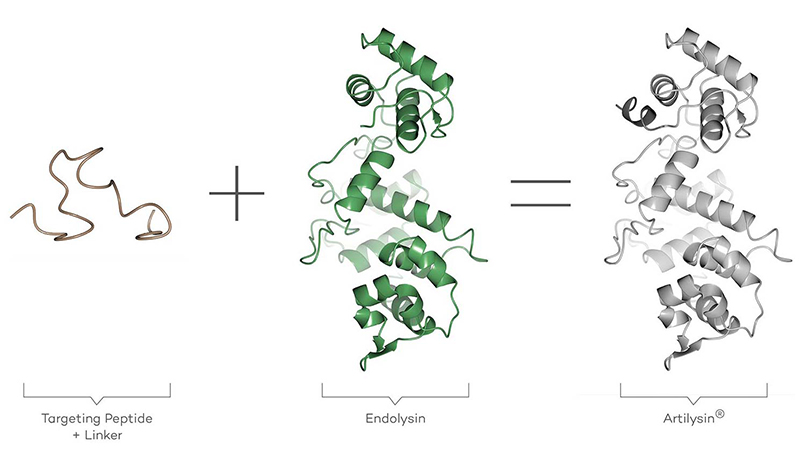
新規エンドリシン®は合成抗菌タンパク質です。基本的な作用機序はエンドリシンと同じですが、生体工学的に改良されており、作用範囲が広くなっています。ペプチド部分が追加された新規エンドリシン®はグラム陰性細菌の外膜を通過し、細胞壁まで到達することができます。そして細胞壁を不安定化させ、細胞内圧(浸透圧)を高めることで細菌の溶解と破裂を引き起こします。内圧の高い車のタイヤに針を突き刺すことを想像してみてください。新規エンドリシン®は細菌に対して同じようなことを行います。このように、新規エンドリシン®はエンドリシンと同じ特徴を持つだけでなく、エンドリシンでは対処できない多剤耐性グラム陰性細菌に対しても有効です。また、複数の例において、新規エンドリシン®はグラム陽性細菌に対してもより効果的でした。
新規エンドリシン®は2009年から世界中の科学者によって開発が続けられています。その新しい分子構造はグラム陽性細菌とグラム陰性細菌の両方に対応しています。また、新規エンドリシン®の基本的な構造はエンドリシンと同じですので、科学者たちは各々の細菌に合わせて理論的に新規エンドリシン®を作ることができます。
新規エンドリシン®は私たちの要求を完全に満たしています。選択的に作用するため、マイクロバイオームを守ることができます。また、あらゆる種類の細菌、多剤耐性菌に対しても有効です。新規エンドリシン®は非常に堅固な細胞構造も攻撃することができるため、細菌が耐性を獲得することは非常に困難です。
新規エンドリシン®はポスト抗生物質の時代に生きる私たちに希望を与えてくれます。
新規エンドリシン®は急速に作用する
新規エンドリシン®は選択的に作用する
結局、私たちにはどのような選択肢があるのでしょうか?
現在、非常に有効な3つの抗生剤があります。いずれも現在主流の抗生物質の代替薬となる可能性があり、また抗生物質よりも効果的かつ安全です。これまで見てきた、バクテリオファージ、エンドリシン、新規エンドリシン®の3つです。
バクテリオファージ
エンドリシン
エンドリシンはとても効果的ですが、すべての細菌に効くわけではありません。特に人間にとって最も脅威の大きいグラム陰性細菌に対して有効性を欠いています。
新規エンドリシン®
新規エンドリシン®はエンドリシンの利点を持ち、さらにあらゆる細菌に対して効果があります。抗生物質の代替薬として現時点では最適です。多くの患者に提供することができ、製薬会社は十分な利益を上げることができます。規制当局から承認を得る必要もありません。細菌が薬剤耐性を獲得するには長い時間がかかります。新規エンドリシン®によって、マイクロバイオームは抗生物質乱用の100年間に受けてきたダメージから回復できます(少なくとも子供や孫たちのマイクロバイオームは)!
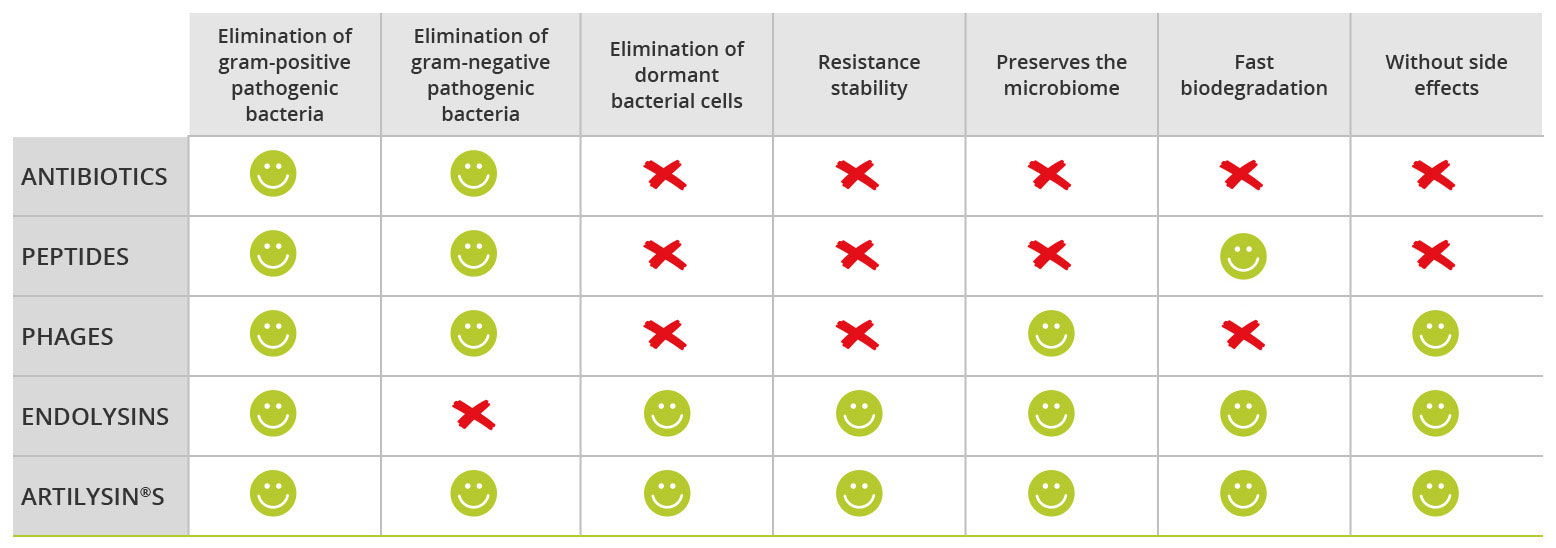
以下の表に抗生物質の代替薬の候補をまとめました。いずれも細菌感染症の治療に用いられることが証明されています。特に今後の発展に重要な特徴について評価しました。
免責事項:このサイトやブログの内容は医学的助言、診断や治療を提供することを意図したものではありません。